シュウ 酸 と 水 酸化 ナトリウム 化学 反応 式
ピースポ 空港 通りシュウ酸と水酸化ナトリウムの中和反応式(COOH)2+2NaOH=2N . シュウ酸と水酸化ナトリウムの中和反応の化学反応式を記せ。 という問題で、答えは、 H₂C₂O₄+2NaOH → Na₂C₂O₄+ 2H₂O なんですが、これはもう覚えるしかないですか? →の左側の式は書けますが、右側は分からなかったです。 まだ右側. 【5分でわかる】中和反応とは?化学反応式と計算問題の解き方 . 塩酸、酢酸、シュウ酸、炭酸などの酸と、アンモニア、水酸化ナトリウムなどの塩基(アルカリ)を用いた中和反応の化学反応式の書き方と具体例と計算方法を解説したうえで、実際の練習問題を通して、自分で解く力をつけましょう。. 高校化学基礎です。シュウ酸と水酸化ナトリウムの中和反応は . つまり、シュウ酸の片方のCOOHのみがナトリウム塩になった状態のものを得たければ、シュウ酸と水酸化ナトリウムの物質量を同じにすれば良い話です。 炭酸塩の場合も同様であり、NaHCO3にNaOHを加えればNa2CO3になります。 NaHCO3で止まっているとするならばその分NaOHが少ないというだけの話です。 当然の事ながら、2価の酸であれば2つの当量点があり、その時のpHは異なります。 シュウ酸の場合にもそうです。 現実問題として、シュウ酸の中和反応を行う時には何らかのpH指示薬を用いて行うことが多いです。 そのとき、シュウ酸は炭酸よりもずっと強い酸ですので、COOHの片方だけが中和された点は、汎用的なpH指示薬の変色域よりも酸性が強く、検出は幾分困難です。. 【高校化学】水酸化ナトリウムはなぜシュウ酸標準溶液で滴定 . シュウ酸標準溶液で水酸化ナトリウムを事前に滴定しなくてはならない理由は、水酸化ナトリウムのとある 2つ の性質に由来します。 1つ目の理由は、 水酸化ナトリウムが潮解性を持つ ということです。. 第23章 実験-中和滴定 - Osaka Kyoiku. 次にシュウ酸と水酸化ナトリウムの反応を考えてみましょう。 (COOH) 2 + 2NaOH → (COONa) 2 + 2H 2 O. ですから,シュウ酸1molに対して,水酸化ナトリウムは2mol必要であることがわかります。 水酸化ナトリウムの濃度を c mol/L,シュウ酸と過不足なく反応した(中和した)水酸化ナトリウム水溶液の体積を V mLとすると, c V /1000=2×5.0×10 -4 の したがって, c =1.0/ v となります。 また,酸と塩基がちょうど中和するとき, (酸の価数)×(酸の物質量)=(塩基の価数)×(塩基の物質量) acV = bcV . の関係がありましたね。 シュウ酸は2価の酸,水酸化ナトリウムは1価の塩基です。. 【公式あり】中和計算を一瞬で解く方法を理由を交えて徹底 . 酸と塩基が反応すると、塩と水H 2 Oが生じる。 この反応を 中和 という。 中和したとき、酸のもつH + と塩基のもつOH ー が1個ずつ組み合わさり、H 2 Oが生じる。 したがって、 「中和する=酸由来のH+と塩基由来のOHーが等しくなる」 と考えることができる。 酸に含まれるH + ・塩基に含まれるOH ー. 酸に含まれるH + 、塩基に含まれるOH ー の物質量 (mol)の求め方、および両者の関係について解説する。 酸に含まれるH+. 硫酸H 2 SO 4 が1molあるとき、そこに含まれるH + は何molだろうか。 H 2 SO 4 は 2価の酸 のため、含まれるH + の物質量 (mol)は、H 2 SO 4 の物質量 (mol)の2倍である。. 中和滴定まとめ(原理・実験レポート考察・器具や指示薬 . 炭酸ナトリウム(Na_2CO_3)と水酸化ナトリウム(NaOH)の混合溶液がある。まず、混合溶液(25 mL)にフェノールフタレインを加え、(0.20 mol/L)の塩酸で滴定したところ終点までに(20 mL)の塩酸を要した。次に、この滴定後にメチル. 【化学基礎】中和の化学反応式の作り方を徹底解説!水ができ . 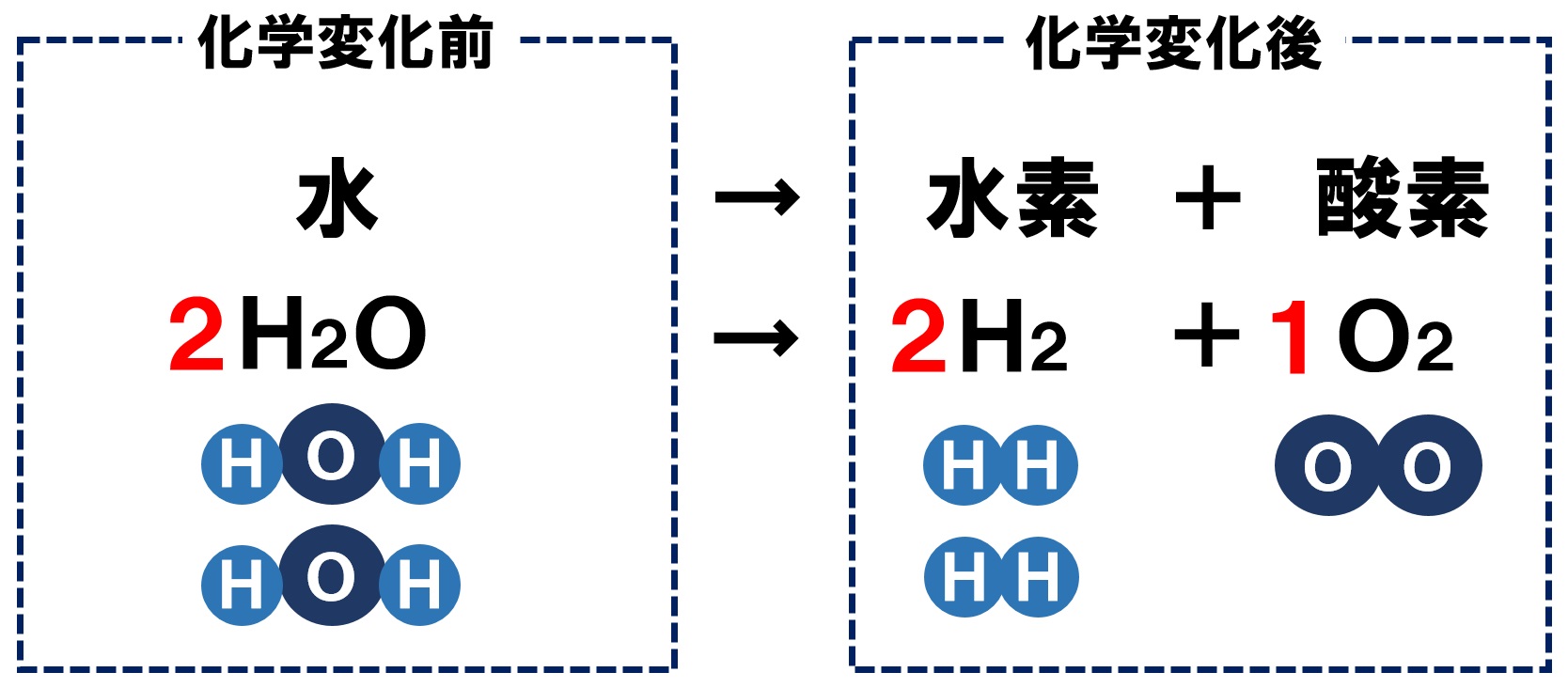
老年 看護 の 役割中和とは,酸とアルカリが反応して,お互いの性質を打ち消し合うこと.. イオンで考えると,水素イオン(H + )と水酸化物イオン(OH - )が反応して,水(H 2 O)ができる反応になります.. 中和. 酸とアルカリが反応して,お互いの性質を打ち消し合うこと.. 両面 テープ どこに 売っ てる
台形 の 土地H + + OH - → H 2 O. 塩(えん) 酸の陰イオンとアルカリの陽イオンでできた物質のこと.. 塩酸と水酸化ナトリウムの中和. 酸である塩酸とアルカリである水酸化ナトリウム水溶液について考えてみましょう.. 塩酸と水酸化ナトリウムは水溶液中で以下のように電離しています.. HCl → H + + Cl -. シュウ酸と水酸化ナトリウムの反応式の作り方を教えて . シュウ酸と水酸化ナトリウムの反応式の作り方を教えてください。 - Clearnote. Clearnote. Q&A. 
霞ヶ浦 高校 落ち た8年弱前. mimi*・☪. シュウ酸と水酸化ナトリウムの反応式の作り方を教えてください。 どうやったら、右辺のようになるってわかるんですか. 質問の言い方が下手でわからなかったら、聞いてください. 回答. ベストアンサー . マロン. 8年弱前. これは酸塩基の中和反応です。 それぞれ水中では. シュウ酸→水素イオンH [+]が2つ、シュウ酸イオンC2O4 [2-] 水酸化ナトリウム→ナトリウムイオンNa [+]、水酸化物イオンOH [-] に電離します。. シュウ酸二水和物(COOH)2・2H2Oと水酸化ナトリウムNaOHの . シュウ酸二水和物 (COOH)2・2H2Oと水酸化ナトリウムNaOHの反応式なのですが… 答えは、 (COOH)2+2NAOH→ (COONA)2+2H2O これは分かるんですけど、シュウ酸二水和物の二水和物はどこへ行ったのですか? また、なぜ書かないのか教えてください。 お願いしますっ。 日本語下手でごめんねなさいいい: ( ;´꒳`;) 化学 ・ 781 閲覧. ベストアンサー. tatsubou さん. 2020/11/7 11:24. 「どこへ行ったか」という質問に対する答えは「周囲の水と混ざって、区別できなくなった」 NEW! この回答はいかがでしたか? リアクションしてみよう. 参考になる. ありがとう. 感動した. 面白い. あわせて知りたい. シュウ酸ナトリウム - Wikipedia. シュウ酸 と 水酸化ナトリウム をモル比 1 対 2 で中和させると、シュウ酸ナトリウムが得られる。 同様にモル比 1 対 1 で反応させると、 シュウ酸水素ナトリウム (NaHC 2 O 4) が得られる。 反応. シュウ酸ナトリウムは 過マンガン酸カリウム 溶液の標定に用いられる。 全ての過マンガン酸イオンと速やかに反応させるため、滴定混合物の温度は60℃以上が望ましい。 この反応の速度論は複雑で、生成したマンガン (II)イオンは過マンガン酸イオンとシュウ酸(硫酸を過剰に加えた溶液中で存在)の反応を触媒するので、滴定してゆくにしたがって反応速度が大きくなる。 最終的な化学反応式は次のとおりである [1] 。 出典. ^ Mcbride, R. S. (1912). 中3化学【中和反応】 | 中学理科 ポイントまとめと整理. 塩酸の化学式はHCl、水酸化ナトリウムの化学式はNaOH。 どちらも代表的な強酸、強アルカリです。 この反応では 塩化ナトリウム NaCl という塩ができています。. シュウ酸ナトリウムの半反応式の作り方 | 化学のグルメ. シュウ酸ナトリウムの半反応式の作り方. 青 の オーブ
御前崎 なぶら 市場 イベントシュウ酸ナトリウムNa 2 C 2 O 4 の半反応式の作り方について、上の5STEPを用いて解説する。 STEP. 酸化剤(還元剤)が「何から何になるのか」を書く。 まずは、酸化剤(還元剤)が「何から何になるのか」を書く。 [ mathrm {C_ {2}O_ {4}^ { ,2-} → CO_ {2}} ] ここは、暗記しておかなければいけない箇所である。 まだ覚えていない場合は次のページを参照のこと。 参考: 半反応式一覧. STEP. 両辺について、OとH以外の原子の数を合わせる。 次に、両辺について、OとH以外の原子の数を合わせる。 [ mathrm {C_ {2}O_ {4}^ { ,2-} → 2CO_ {2}} ]. 中和反応式 一覧‥中和反応でできる『塩の種類と性質』|中学 . 2022.05.31. スポンサーリンク. 中和反応の基本. 中和とは? 酸性の水溶液とアルカリ性の水溶液を混ぜ合わせたときに反応して互いに性質を打ち消し合う反応をいいます。 その結果、 塩 (えん)と水 が発します。 酸 + アルカリ(塩基) → 塩 + 水. 塩 とは? 中和反応の際、酸の水素イオン、塩基の水酸化物イオンから水が生じます。 残りの酸の陰イオンとアルカリ(塩基)の陽イオンが結合してできる物質を塩といいます。 中和反応でできる塩の種類 早見表. 水酸化ナトリウム. 水酸化カリウム. 水酸化バリウム. 水酸化カルシウム. アンモニア水. 《NEXT:中和反応の化学式 一覧》 ホーム. 中学. 理科. 中和反応式25種類を一覧と早見表で紹介しています。. シュウ酸 - Wikipedia. 実験的には、ギ酸ナトリウムを加熱分解して生成するシュウ酸ナトリウムを、水酸化カルシウムによってシュウ酸カルシウムとして単離し、これを硫酸で分解することで得られる。. 酸化還元反応式の作り方 | 理系ラボ. 酸化剤と還元剤を用いて酸化還元反応を表した式のことを 酸化還元反応式 といいます。「酸化数とは(求め方・計算問題)」の記事で半反応式について解説しましたが、酸化剤の半反応式と還元剤の半反応式を組み合わせることによって. 【高校無機化学】酸化物の分類、酸化物と水の反応 | 受験の月. 酸化物の分類非金属}の酸化物 酸性}酸化物 {NO₂}, CO₂, {SO₃}, {SO₂ 金属}の酸化物 塩基性}酸化物 {Na2O}, {K2O}, {CaO}, {BaO 塩基性酸化物}+水} 水酸化物$} Na2O+H₂O} {2}{NaOH$ ${CaO+H₂O} {Ca(OH)₂. 水酸化ナトリウムの性質と反応 | ネットdeカガク. 化学式: NaOH. 融点 : 318.4℃. 密度 : 2.13. pKa : 13. 溶解度 :水に溶解 (0℃ .42g/mL, 100℃ 3.47g /mL) 吸湿性・潮解性があるので秤量はすばやく行う. 水酸化ナトリウム水溶液の調製方法. 水酸化ナトリウムの水溶液を調製することはたくさんあります。 10%NaOHのように質量パーセント濃度で指定されたり、1 mol/L (1M)NaOHなどモル濃度で指定されている例があります。 使用用途によって、どの程度厳密な濃度の水溶液を用意する必要があるかが変化します。 滴定やpH測定の校正などの分析利用する場合は正確な濃度を用意しましょう。 一方で塩基性水溶液で分液する時などでは精密な濃度調製は求められません。. 【還元剤】シュウ酸(Cooh)2の半反応式の作り方 | ねこでも . なぜ炭酸ナトリウムNa2CO3と二酸化炭素CO2と水H2Oが反応すると炭酸水素ナトリウムNaHCO3が生じるの? なぜ水酸化ナトリウムNaOHは潮解性があるの? なぜ炭酸水素ナトリウムNaHCO3を加熱すると炭酸ナトリウムNa2CO3が生じるの?. シュウ酸の半反応式の作り方 | 化学のグルメ. シュウ酸の半反応式の作り方. シュウ酸H 2 C 2 O 4 の半反応式の作り方について、上の5STEPを用いて解説する。 STEP. 酸化剤(還元剤)が「何から何になるのか」を書く。 まずは、酸化剤(還元剤)が「何から何になるのか」を書く。 [ mathrm {H_ {2}C_ {2}O_ {4} → CO_ {2}} ] ここは、暗記しておかなければいけない箇所である。 まだ覚えていない場合は次のページを参照のこと。 参考: 半反応式一覧. STEP. 両辺について、OとH以外の原子の数を合わせる。 次に、両辺について、OとH以外の原子の数を合わせる。 [ mathrm {H_ {2}C_ {2}O_ {4} → 2CO_ {2}} ] STEP. 【中学 理科】中和反応(塩酸と水酸化ナトリウム) - YouTube. 0:00 / 39:03. 中学理科・化学単元より中和反応の授業動画です。 基本となる塩酸と水酸化ナトリウムの反応をイオンの図解をまじえて紹介しました。 初学の方・試験前の復習にご覧いただけたら幸です。 チャンネル登録・評価いただけると喜びます。 ーーーーーーーーーーーーーーーーーーーーーーーーーーーーーーーー【フジキン学院 プロフィール】こんに. 【中3理科一問一答】酸とアルカリ・中和・イオンの一問一答 . 
たつの 救急 病院反応により炭酸カリウムが形成された, 二酸化塩素, 二酸化炭素と水. この反応は、二酸化塩素の実験室合成に使用されます. 3. シュウ酸の反応 c アンモニア溶液: c2h2o4 + 2nh3→ (nh4)2c2o4. シュウ酸は水に溶けた . アルミニウムと水酸化ナトリウムの反応・化学反応式 - ノリックジオグラフィック. Step1: 酸化アルミニウムの溶解: このステップで、アルミニウムの表面の酸化アルミニウムが水酸化ナトリウムと反応してテトラヒドロキシドアルミニウムイオンを形成します。. Al₂O₃ (s) + 2NaOH (aq) + 3H₂O (l) → 2Na [Al (OH)₄] (aq) Step2: アルミニウムの反応 . 化学式・化学反応式の違いについて分かりやすく解説!【中学 理科】|かめのこブログ. 1. 化学式と化学反応式の違い. まずは、簡単に「化学式」と「化学反応式」の違いを理解しましょう!! ① 化学式とは 「 化学式 」とは、「物質を元素の構成で表したもの」のことです 。 化学式では、物質を構成する元素の記号とその数で表します。. 酸化還元反応の化学反応式一覧(問題と答え)【化学反応式の王道】 | 大学受験の王道. 自己酸化還元反応。. ⑨硫黄と酸素. S + O2 → SO2. ※接触法の一段階目の反応。. ⑩黄鉄鉱を燃焼させる。. 4FeS2 + 11O2 → 2Fe2O3 + 8SO2. ※接触法の一段階目の反応として、硫黄の燃焼ではなく、黄鉄鉱を燃焼させて二酸化硫黄を得ることもある。. ⑪二酸化硫黄と . 水と水酸化ナトリウムの反応式を教えてください。 - 物を造るとき. - Yahoo!知恵袋. 2007/12/16 12:21. 3 回答. 水と水酸化ナトリウムの反応式を教えてください。. 物を造るときに90℃のお湯13.5ℓに水酸化ナトリウム1.5kg投入し、溶液を調整するとします。. この時非常に大きな熱が発生し突沸するということは周知の事実であると思います。. この . フタル酸水素カリウム水溶液を水酸化ナトリウムで滴定した時の化学反応式がわか. - Yahoo!知恵袋. フタル酸水素カリウム水溶液を水酸化ナトリウムで滴定した時の 化学反応式がわかりません。 c6h4(cooh)(c フタル酸水素カリウム水溶液を水酸化ナトリウムで滴定した時の 化学反応式がわかりません。 c6h4(cooh)(cook)+naoh→? どなたか教えていただけませんか?. スマナビング!高校数学/物理/化学と線形代数をスマホで学ぶサイト. 理論化学. 酸塩基; 酸化還元反応; . 数学2:「図形と方程式」とその関連分野を解説した記事や公式、解放のコツなどをまとめました。 . 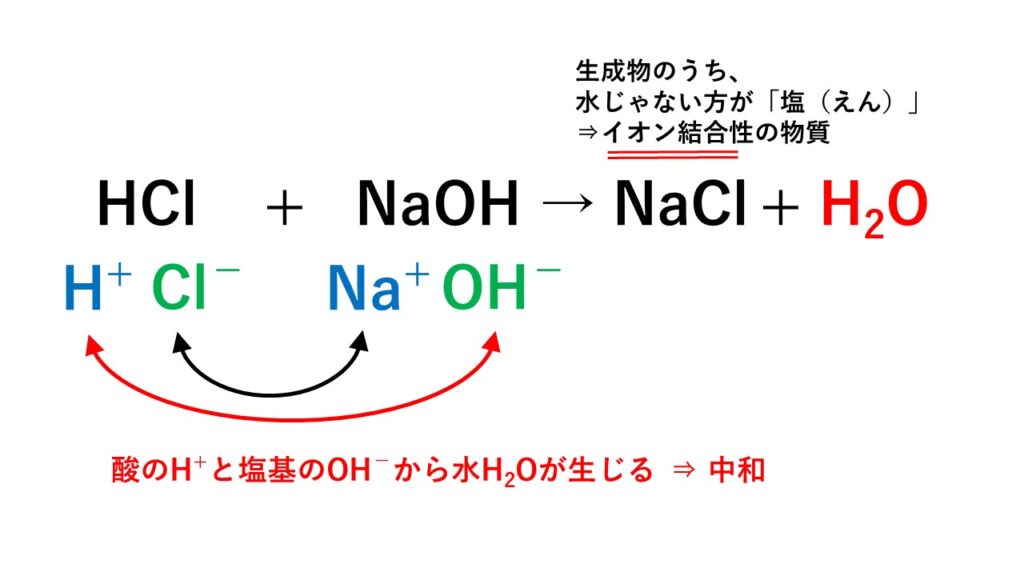
日本 空手 協会 帯 の 色そしてこのこの3つの物質の関係性を表すと次のように式にすることができるよ。. Fe + S → FeS. これが鉄と硫黄の化学反応式 だよ。. この式を見れば、. 「鉄 に 硫黄 を加えると 硫化鉄になる」という関係が分かるよね。. 運命 の 出会い ガシャ
クリスタ 落ち た 復元式には、記号が使われているね . 水酸化ナトリウム(NaOH)とクエン酸(C6H8O7)の反応式を教えてくだ. - Yahoo!知恵袋. 水酸化ナトリウム(NaOH)とクエン酸(C6H8O7)の反応式を教えてくださいm(__)m クエン酸には、カルボキシル基(COOH基)が3つあるので、C6H8O7+3NaOH→C6H5O7Na3+3H2Oとなります。(補足についてです)2AgNO3+K2CrO4→Ag2CrO4+2KNO3赤褐色のクロム酸銀が沈殿します。. 硫酸と水酸化ナトリウムの中和・反応式は? | 令和の知恵袋. 硫酸と水酸化ナトリウムの中和・反応式は? 硫酸と水酸化ナトリウムが中和する化学反応式について、h2so4は二価の酸のため、2h(+)+so4(-)のようになります。 なので、次のような反応式となります。 h2so4+2naoh→na2so4+2h2o. 硫酸h2so4は、水素イオンh+ を2個持ちます。. 酸化還元滴定(実験・計算問題・指示薬・硫酸酸性にする理由など) | 化学のグルメ. はじめに 【プロ講師解説】このページでは『酸化還元滴定(実験・計算問題・指示薬・硫酸酸性にする理由など)』について解説しています。. 酸化還元滴定の流れ ここに、濃度未知の還元剤であるシュウ酸H2C2O4(無色)が入った容器があるとする(シュ. 化学反応式 - 二酸化炭素と水酸化ナトリウムの中和の化学反応式を教えてく. - Yahoo!知恵袋. 化学反応式 二酸化炭素と水酸化ナトリウムの中和の化学反応式を教えてください。生じる塩がわからなくて困っています。。 あまり見たことのない化学反応ですが、もっともらしい答えはCO2+NaOH→NaHCO3ですかね。二酸化炭素の水溶液と考えると、わかりやすいかも。CO2+H2O→H2CO3 . 半反応式の覚え方と作り方|酸化剤・還元剤の半反応式の一覧. 半反応式の一覧. 酸化還元反応の反応式は 半反応式 がベースにあるため,酸化還元反応の反応式がどうなるかを知るためには半反応式が書ける必要があります.. そこで,よく扱われる典型的な半反応式はきちんとフォローしておくことが大切で,以下の . シュウ酸水溶液と水酸化ナトリウム水溶液の中和反応の化学反応式を教えて. - Yahoo!知恵袋. シュウ酸と水酸化ナトリウムの中和反応の式なのですが、水酸化ナトリウムの係数2はどういうことでしょ. ベストアンサー:Oの数は合っていますよ。. 左辺のシュウ酸H₂C₂O₄にOは4、2NaOHにOは2、合わせて6。. 右辺のNa₂C₂O₄nOは4、2H₂OにOは2、合わせて6 . 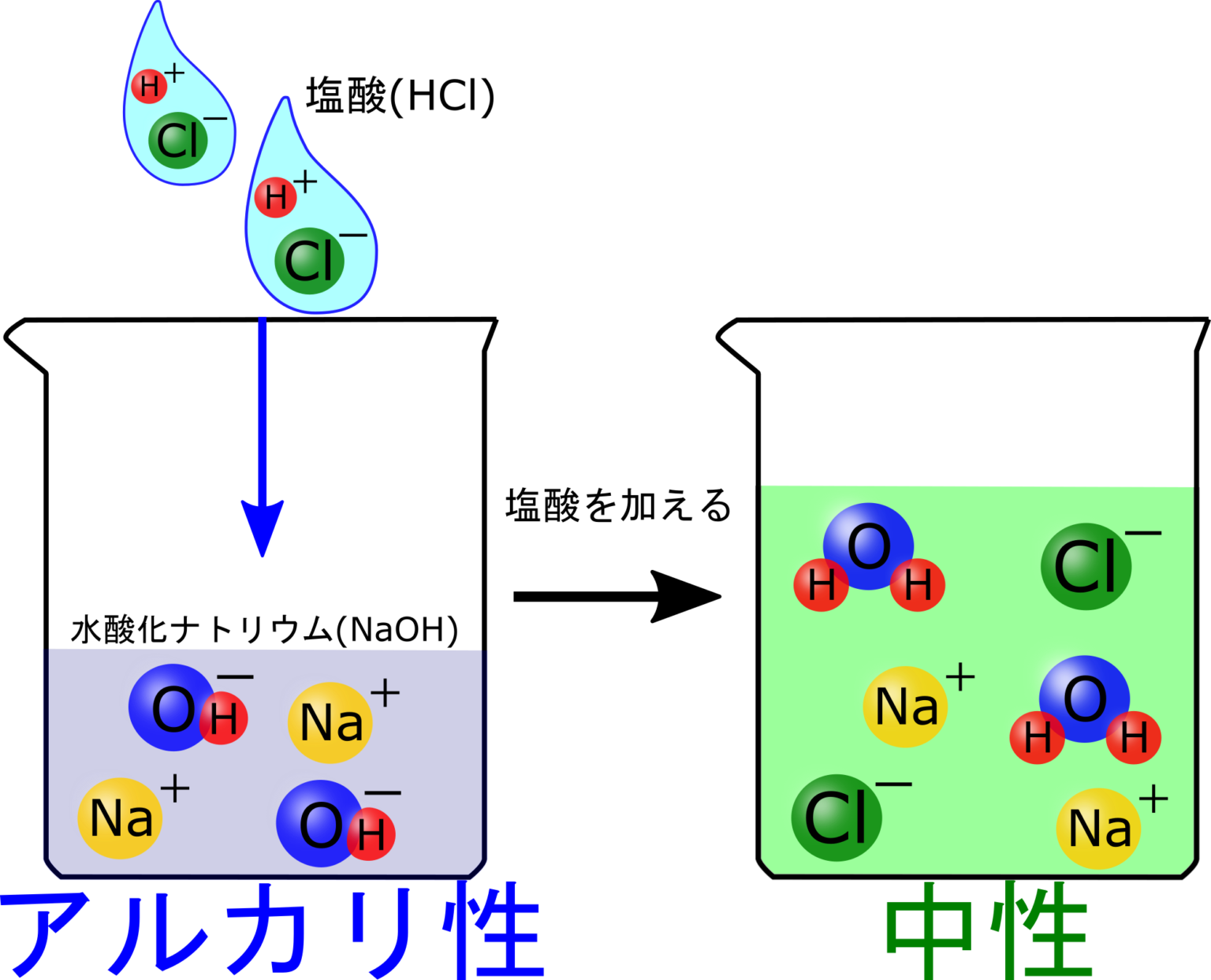
排水 溝 下水 の 匂いケイ素 化合物 化学 単体 性質 無機化学 製法. 気に入ったらシェアしてね!. はじめに 【プロ講師解説】このページでは『ケイ素の単体と化合物の性質・製法』について解説しています。. ケイ素の単体 ケイ素Siの単体の特徴は次の通りである。. ケイ素Siの . 漂白剤で洗濯物が白くなる理由、化学反応式について解説【高校生の身近な科学】 │リケラボ. 漂白剤とは?. 漂白剤を一言でいうと「汚れの色素を化学反応で白く変化させる働きをもつ成分」のこと。. よく「漂白剤は服自体を白くする」と勘違いしている方がいますが、基本的には汚れの色素に対して反応させる目的で使用します。. 一方、洗濯洗剤 . 屋上 の ある 家 980 万 円
くま の キャラクター 一覧化学反応式一覧(理論化学・無機化学)【大学受験】 | 大学受験の王道. ☆解説授業一覧はこちら→化学反応式の王道の解説動画・授業動画一覧 (1)中和と電離. ①塩酸と水酸化ナトリウム. hcl + naoh → nacl + h 2 o. ②酢酸の電離. ch 3 cooh ⇄ ch 3 coo - + h +. ③アンモニアの電離. 銀鏡反応の原理と反応式について解説|科学探偵の日常の謎解き. (反応式) ag 2 o+4nh 3 +h 2 o→2[ag(nh 3) 2] + +2oh - ③ビーカーに②の溶液とグルコース(アセトアルデヒド、ホルマリンでもアルデヒド基を持つ化合物)を入れて、さらに水酸化ナトリウムを加えてアルカリ性にして、50~60℃のお湯につけて、銀を析出させる。. 両性元素とは(ゴロ・覚え方・反応式など) | 化学のグルメ. 
化学反応式 -水酸化ナトリウムと塩素の反応は 2NaOH+Cl2→NaCl- | OKWAVE. 化学反応式. 水酸化ナトリウムと塩素の反応は 2NaOH+Cl2→NaClO+NaCl+H2Oで表され、そしてここで塩酸を加えると NaClO+HCl→HClO+NaCl HClO+HCl→Cl2+H2Oという風に反応は進んでいくらしいのですが、このような化学反応式はどのようにして導けばいいのでしょう . ヨウ素の酸化還元反応、ヨウ素酸化滴定、ヨウ素還元滴定の原理を基本から解説 | ジグザグ科学.com. 本記事はヨウ素の酸化還元反応とヨウ素滴定について、わかりやすくまとめた記事です。ヨウ素滴定には、主にヨウ素酸化滴定とヨウ素還元滴定があります。この記事を読んで理解すると、ヨウ素の酸化還元反応とそれを利用した滴定法について理解を深めることができます。. 化学反応式(係数・作り方・書き方・計算問題の解き方など). 化学反応式と単位計算. ここからは、化学反応式を使った計算問題の解き方について解説する。 まずはじめに、化学反応式について1つ押さえておくべきことがある。 係数比=モル比. 化学反応式における係数の比はモル比を表している。. 油脂(構造・酸化・加水分解・グリセリンや脂肪酸との関係など) | 化学のグルメ. はじめに 【プロ講師解説】このページでは『油脂(構造・酸化・加水分解・グリセリンや脂肪酸との関係など)』について解説しています。 油脂とは グリセリン1分子に高級脂肪酸3分子が結合した3価のエステル(トリグリセリド)を油脂という。 油脂は3. 【高校化学】#05酸化還元の反応式とは → High Chemi 【テスト対策】. ① 酸化剤・還元剤の半反応式を用意する。 ② e − の係数を合わせるために、それぞれの係数の最小公倍数になるよう全体の係数をかける。 ③ 2式を足す。 ④ 半反応式を作る際に消したイオンがあれば元に戻し、右辺のイオンは他のイオンと合成する。. 【高校化学基礎】「中和反応」 | 映像授業のTry IT (トライイット). 先ほどの中和反応を、化学反応式で見てみましょう。 HCl+NaOH→NaCl+H 2 O ここで、HClは 酸 、NaOHは 塩基 、H 2 Oは 水 ですね。 そして、NaClは 塩(えん) と呼ばれます。 酸の陰イオンと塩基の陽イオンが結合したものを、塩というわけです。.